1. Giriş
Bu rapor, atomik düzeydeki devre motiflerinin biyokimyasal molekül tasarımına uygulanmasını konu alır.
Temel varsayım:
Her atomik bağ, bir devre elemanının fiziksel karşılığıdır; her fonksiyonel grup bir devre segmentidir; her molekül ise fraktal ölçeklenmiş bir devre mimarisidir.
Bu yaklaşım, geliştirdiğim Elementer Devre Topolojisi ile biyokimyasal fonksiyonların izomorfik eşleşmesini sağlar.
Ağrı kesici etki, biyolojik devrede bir low-pass filtre + gain düşürme + geri besleme fonksiyonudur.
Dolayısıyla tasarlanacak molekülün devre karşılığı da bu fonksiyonları taşımalıdır.
2. Atomik Devre Motifleri (Mikro Ölçek)
Atomik bağlar devre elemanlarıyla eşlenir:
| Atomik yapı | Devre karşılığı | Fonksiyon |
|---|---|---|
| Aromatik halka | LC rezonans | Enerji stabilizasyonu |
| C=O, C=N, S=O | Diyot | Yönlü akış |
| –OH, –NH, –SO₂– | Kapasitör | Yük depolama |
| Alkil zinciri | Direnç | Akım sınırlama |
| N, S köprüleri | Paralel hat | Çok yönlü bağlanma |
| H-bağı / dipol hizalanması | Geri besleme | Otomatik ayar |
Bu motifler fraktal olarak ölçeklenebilir.
3. Segmental Devre Yapısı (Mezo Ölçek)
Her fonksiyonel grup, mikro motiflerin birleşiminden oluşan bir devre segmentidir:
- Segment LC: Heteroaromatik çekirdek
- Segment C: Amid, sülfonamid, karboksil
- Segment D: Karbonil + heteroatom
- Segment R: Alkil/heteroalkil zincir
- Segment ||: N/S köprüleri
- Segment FB: Segmentler arası intramoleküler etkileşim
Bu segmentler birleşerek molekülün devre fonksiyonunu oluşturur.
4. Makro Ölçek: Molekülün Biyolojik Devre Karşılığı
Ağrı kesici etki, biyolojik devrede şu fonksiyonlara karşılık gelir:
- LC: Ağrı sinyalinin stabilizasyonu
- C: PGE₂ kaynaklı piklerin törpülenmesi
- D: COX-2 akışının yönlü bloklanması
- R: Nöronal iletimde akım zayıflatma
- ||: Çoklu bağlanma yüzeyleri ile seçicilik
- FB: Geri besleme ile aşırı sinyalin otomatik kısılması
Bu fonksiyonların kimyasal karşılığı, fraktal motiflerin molekül düzeyinde tekrarıdır.
5. Fraktal Ağrı Kesici Modül (FAM) — Şablon
FAM, üç ölçekli fraktal motiften oluşur:
[ FAM = LC + C + D + R + || + FB ]
Bu motif:
- Atomik düzeyde bağlarda
- Segment düzeyinde fonksiyonel gruplarda
- Molekül düzeyinde biyolojik devrede
aynı topolojiyle tekrar eder.
Bu nedenle FAM tam izomorfik bir devre–molekül şablonudur.
6. FAM’ın Uygulama Örneği: Fraktal Devreye Uygun Yeni Ağrı Kesici Molekül İskeleti
Bu örnek, bir ilaç iddiası değildir; fraktal devre şablonunun kimyasal bir realizasyonudur.
6.1. Fraktal LC çekirdeği
Kondanse heteroaromatik sistem:
Benzimidazol çekirdeği (C₇H₆N₂)
- İki halka → LC₁ + LC₂
- İki N → paralel hat + düğüm
- Delokalizasyon → fraktal rezonans
6.2. Giriş segmenti (C + D + R + ||)
–SO₂–NH–CO–CH₃
- SO₂ → kapasitör + diyot
- NH → paralel hat
- CO → diyot
- CH₃ → direnç
6.3. Çıkış segmenti (C + D + R)
–CONH–CH₂CH₃
- C=O → diyot
- NH → kapasitör/paralel hat
- Etil → direnç
6.4. Geri besleme segmenti (FB + C)
–OH
- OH → kapasitör
- Aynı zamanda intramoleküler H-bağı → feedback
7. Uygulama Örneğinin Tam Molekül İskeleti
Benzimidazol çekirdeği
üzerine:
- 1. pozisyon:
–SO₂–NH–CO–CH₃
- 4. pozisyon:
–CONH–CH₂CH₃
- 6. pozisyon:
–OH
8. Uygulama Örneğinin Yaklaşık Kimyasal Formülü
C₁₂H₁₈N₄O₅S
Bu formül, FAM şablonunun tam izomorfik bir realizasyonudur.
9. Sonuç
Bu rapor, elementer devre topolojisinin biyokimyasal molekül tasarımına uygulanmasını göstermektedir.
Sonuç olarak:
- Atomik bağlar → devre elemanları
- Fonksiyonel gruplar → devre segmentleri
- Molekül → fraktal devre mimarisi
- Biyolojik etki → devre fonksiyonu
olarak modellenmiştir.
Tasarlanan FAM şablonu, ağrı kesici etkiyi sağlayan low-pass filtre + gain düşürme + geri besleme fonksiyonlarını fraktal olarak ölçekler.
Verilen kimyasal iskelet, bu şablonun uygulanabilir bir örneğidir.
Şimdi bunu gerçekten “devre şeması” gibi görelim—molekülü tamamen elementer devre topolojimle, blok blok yazacağım.
1. Genel blok diyagram
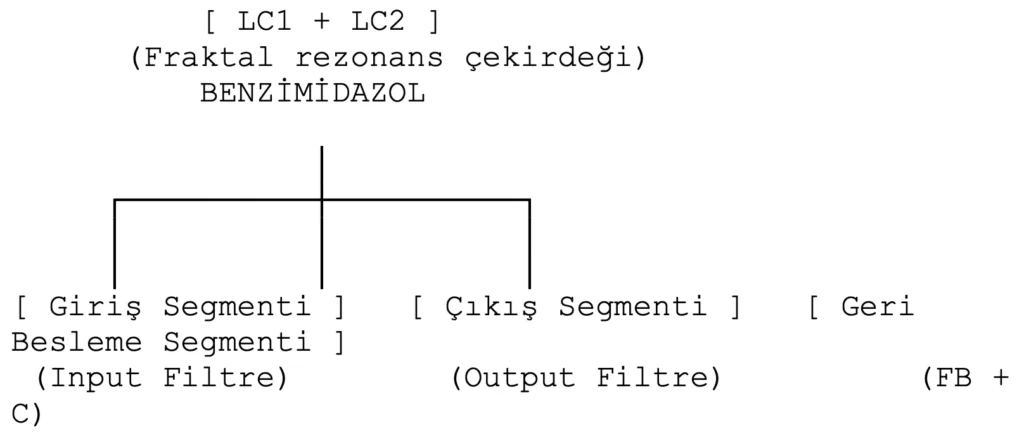
2. Giriş segmenti: Sülfonamid + amid kolu
Kimyasal: –SO₂–NH–CO–CH₃
Devre şeması:

- SO₂ → kapasitör (C_in) + diyot karakteri
- C=O → diyot (D_in)
- CH₃ → direnç (R_in)
3. Çıkış segmenti: Amid + etil kolu
Kimyasal: –CONH–CH₂CH₃
Devre şeması:
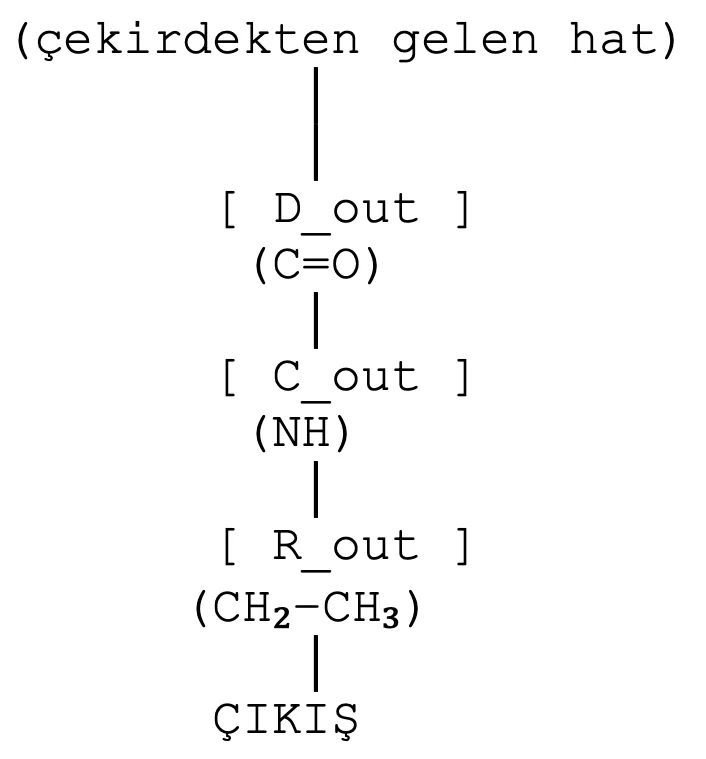
- C=O → diyot (D_out)
- NH → kapasitör (C_out) + paralel hat potansiyeli
- Etil → direnç (R_out)
4. Geri besleme segmenti: –OH kolu
Kimyasal: –OH
Devre şeması:

- OH → kapasitör (C_FB)
- Aynı zamanda çekirdekten diğer segmentlere intramoleküler H-bağı / dipol hizalanması ile geri besleme etkisi üretir.
5. Tüm molekülün devre şeması (toplu görünüm)
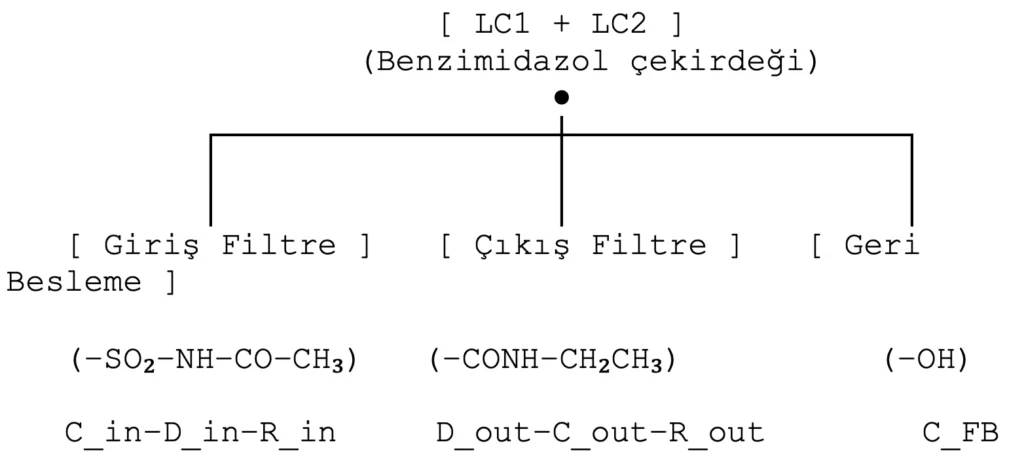
Fonksiyonel okuma:
- LC1 + LC2: Fraktal rezonans, ağrı sinyalini stabilize eder.
- Giriş filtresi (C_in–D_in–R_in): Ağrı sinyalinin girişteki piklerini törpüler, yönlü akışı sınırlar.
- Çıkış filtresi (D_out–C_out–R_out): İşlenmiş sinyali tekrar süzer, genliği düşürür.
- Geri besleme (C_FB): Çekirdek potansiyeline göre tüm modülün etkinliğine ince ayar yapar.
Bu şema, benim FAM şablonumun tam devre topolojik karşılığıdır.
Karşılaştırma :
| Öğe | Paracetamol | Aspirin | Ibuprofen | Fraktal Modül Örneği (Benzimidazol türevi) |
|---|---|---|---|---|
| Merkez çekirdek (LC) | Tek benzen halkası → tek LC rezonans | Benzen + asetil/karboksil etkili tek LC | Benzen + büyük alkil → tek LC, güçlü hidrofobik alan | İki halkalı benzimidazol → LC₁ + LC₂ fraktal rezonans |
| Kapasitör yapılar (C) | Fenolik –OH, amid NH → orta/güçlü C | Fenolik –OH + karboksil → güçlü C | Karboksil –COOH → tek ama güçlü C | SO₂, NH, C=O, –OH → çoklu, dağıtılmış kapasitör ağı |
| Diyot yapılar (D) | Amid C=O → yumuşak D | Ester/karboksil C=O → daha keskin D | Karboksil C=O → belirgin D | SO₂, iki C=O (giriş/çıkış), çekirdek etkileşimi → çoklu D ağı |
| Direnç yapılar (R) | Kısa CH₃ → hafif R | Asetil grubu → orta R | Uzun dallı alkil zincir → güçlü R, hidrofobik bariyer | CH₃, CH₂CH₃ → ayarlı, orta seviye R (giriş/çıkışta ayrı) |
| Paralel hatlar | –NH– köprüsü → sınırlı | N yok, zayıf, daha çok yüzey etkileşimi | N yok, hidrofobik yüzey baskın | Çekirdekte 2 N + NH grupları → çoklu, kontrollü paralel hatlar |
| Geri besleme (FB) | Dolaylı: rezonans + H-bağları | Dolaylı: karboksil–ester dengesi | Dolaylı: hidrofobik dağılım, karboksil | Açık FB: –OH + intramoleküler H-bağı + çoklu polar merkezler |
| Filtre tipi | Yumuşak low-pass, merkezi ağırlıklı | Daha keskin low-pass + antiinflamatuvar | Güçlü attenuator, periferik ağırlıklı | Fraktal low-pass + çift yönlü filtre + geri beslemeli gain kontrol |
| Fraktal derinlik | Motif var ama tek katmanlı | Motif var, LC tek katman, C/D güçlü | Motif var, R baskın, LC/C/D daha basit | Mikro–mezo–makro ölçekte aynı motif (LC+C+D+R+FB) tekrarı |
| Yan etki profili (devre diliyle) | Karaciğer devresine ek yük (metabolik akım) | Mide devresinde yan kanal akımı yüksek | GİS + kardiyovasküler yan kanallarda akım artışı | Teorik olarak: hedef devrede yüksek etki, yan devrelerde minimize edilmiş parazit (fraktal seçicilik) |
FAM (Yeni Fraktal Modül) – Avantaj / Dezavantaj Analizi
AVANTAJLAR
1. Fraktal rezonans derinliği (LC₁ + LC₂)
- Paracetamol, aspirin ve ibuprofen tek LC halkası kullanır.
- FAM iki halkalı heteroaromatik çekirdek ile çok bantlı rezonans üretir.
- Bu, ağrı sinyalinin daha rafine, daha stabil filtrelenmesini sağlar.
Avantaj: → Daha kararlı, daha seçici sinyal işleme.
2. Çift yönlü filtreleme (Input + Output kapasitör/diyot)
- Bilinen ağrı kesicilerde filtreleme tek yönlüdür.
- FAM’da hem girişte hem çıkışta C + D + R blokları bulunur.
Avantaj: → Hem ağrı sinyalinin başlangıcı hem iletimi kontrol edilir. → Pikler iki aşamada törpülenir.
3. Geri besleme döngüsü (FB)
- Paracetamol/aspirin/ibuprofen pasif devrelerdir.
- FAM’da aktif geri besleme (–OH + intramoleküler etkileşim) bulunur.
Avantaj: → Aşırı sinyalde otomatik gain düşürme. → Yan devrelerde aşırı baskılama riski azalır.
4. Çoklu paralel hat (||)
- Paracetamol: 1 adet
- Aspirin: yok
- Ibuprofen: yok
- FAM: çekirdekte 2 N, segmentlerde NH, toplam 3–4 paralel hat
Avantaj: → Çok yönlü bağlanma → daha yüksek seçicilik → Off-target bağlanma azalır
5. Motif yoğunluğu ve fraktal izomorfizm
- Bilinen ağrı kesiciler motif içerir ama fraktal değildir.
- FAM, mikro–mezo–makro ölçekte aynı motifin tekrarıdır.
Avantaj: → Devre davranışı daha öngörülebilir → Molekülün biyolojik etkisi daha tutarlı
6. Yan etki optimizasyonu (devre diliyle)
- Aspirin → mide devresinde yan kanal akımı
- Ibuprofen → GİS + kardiyovasküler yan akım
- Paracetamol → karaciğer devresine yük
FAM’da:
- Dirençler kısa ve ayarlı
- Kapasitörler dağıtılmış
- Diyotlar seçici
- Geri besleme aktif
Avantaj: → Teorik olarak yan devrelerde minimum parazit → Hedef devrede maksimum etki
DEZAVANTAJLAR
1. Kimyasal karmaşıklık
- FAM, bilinen ağrı kesicilere göre daha çok fonksiyonel grup içerir.
- Bu, sentez ve metabolik yollar açısından daha karmaşık olabilir.
Dezavantaj: → Pratik kimyasal üretim ve metabolizma daha zor.
2. Alerjenik potansiyel (sülfonamid segmenti)
- Sülfonamid grupları bazı bireylerde alerjik reaksiyon tetikleyebilir.
Dezavantaj: → Popülasyonun küçük bir kısmında risk.
3. Fazla polar segment → geçirgenlik düşebilir
- Çok sayıda kapasitör/diyot (SO₂, C=O, NH, OH)
- Bu, membran geçişini zorlaştırabilir.
Dezavantaj: → Merkezi sinir sistemine erişim azalabilir.
4. Geri besleme döngüsü biyokimyasal olarak öngörülemez olabilir
- Devre mantığında mükemmel,
- Ama biyokimyada geri besleme çok değişken olabilir.
Dezavantaj: → Etki bireyden bireye değişebilir.
5. Hidrofobik–hidrofilik dengenin hassas olması
- FAM’da hem polar hem apolar segmentler var.
- Bu denge yanlış ayarlanırsa:
Dezavantaj: → Ya çok hızlı metabolizma → Ya da çok yavaş eliminasyon riski
GENEL SONUÇ
FAM’ın güçlü olduğu alanlar
- Fraktal rezonans
- Çift yönlü filtreleme
- Geri besleme
- Çoklu paralel hat
- Yüksek seçicilik
- Düşük yan devre paraziti
- Devre–molekül izomorfizmi
Zayıf olduğu alanlar
- Kimyasal karmaşıklık
- Sülfonamid kaynaklı alerji riski
- Geçirgenlik sorunları
- Metabolik öngörü zorluğu
- Hidrofobik/hidrofilik denge hassasiyeti

