1. 引言
本报告讨论了原子级电路模板在生化分子设计中的应用。
基本假设:
- 每个原子键是电路元件的物理对应物
- 每个官能团是电路段
- 每个分子是分形缩放的电路架构
这种方法通过我提出的基本电路拓扑实现了生化功能的同构匹配。
例如,止痛作用在生物电路中对应于低通滤波器 + 增益衰减 + 反馈功能。
因此,所设计分子的电路对应也应包含这些功能。
2. 原子电路模板(微观尺度)
原子键对应于电路元件:
| 原子结构 | 电路对应 | 功能 |
|---|---|---|
| 芳环 | LC 共振 | 能量稳定 |
| C=O, C=N, S=O | 二极管 | 定向流 |
| –OH, –NH, –SO₂– | 电容 | 电荷存储 |
| 烷基链 | 电阻 | 电流限制 |
| N, S 桥 | 并联线 | 多向连接 |
| 氢键 / 偶极对齐 | 反馈 | 自动调节 |
这些模板可分形缩放。
3. 电路段结构(中观尺度)
每个官能团由微观模板组合而成,形成电路段:
| 段 | 组成 |
|---|---|
| LC 段 | 杂芳环核心 |
| C 段 | 酰胺、磺酰胺、羧基 |
| D 段 | 羰基 + 杂原子 |
| R 段 | 烷基/杂烷基链 |
| FB 段 | 分子内段间相互作用 |
这些段组合形成分子的电路功能。
4. 宏观尺度:分子的生物电路对应
止痛作用在生物电路中对应功能:
| 电路功能 | 生物对应 |
|---|---|
| LC | 稳定疼痛信号 |
| C | 平滑 PGE₂ 引起的峰值 |
| D | 定向阻断 COX-2 流 |
| R | 在神经传导中衰减电流 |
| FB | 反馈自动抑制过强信号 |
这些功能的化学对应是分形模板在分子层面的重复。
5. 分形止痛模块 (FAM) — 模板
FAM 由三层分形模板组成:FAM=LC+C+D+R+∣∣+FB
此模板在:
- 原子级键
- 官能团段
- 分子级生物电路
都以相同拓扑重复。
因此,FAM 是完全同构的电路-分子模板。
6. FAM 应用示例:分形电路的新止痛分子骨架
此示例不是药物声明,而是分形电路模板的化学实现。
6.1 分形 LC 核
浓缩杂芳环系统:
- 苯并咪唑核心 (C₇H₆N₂)
- 两环 → LC₁ + LC₂
- 两个 N → 并联线 + 节点
- 离域化 → 分形共振
6.2 输入段 (C + D + R + ||)
−SO2–NH–CO–CH3
- SO₂ → 电容 + 二极管
- NH → 并联线
- CO → 二极管
- CH₃ → 电阻
6.3 输出段 (C + D + R)
−CONH–CH2CH3
- C=O → 二极管
- NH → 电容 / 并联线
- CH₂CH₃ → 电阻
6.4 反馈段 (FB + C)
−OH
- OH → 电容
- 同时分子内氢键 → 反馈
7. 应用示例完整分子骨架
苯并咪唑核心,上面连接:
- 1 位:−SO2–NH–CO–CH3
- 4 位:−CONH–CH2CH3
- 6 位:−OH
8. 应用示例近似化学式C12H18N4O5S
该分子是 FAM 模板的完全同构实现。
9. 结论
本报告展示了基本电路拓扑在生化分子设计中的应用。
总结如下:
- 原子键 → 电路元件
- 官能团 → 电路段
- 分子 → 分形电路架构
- 生物作用 → 电路功能
设计的 FAM 模板以分形方式缩放低通滤波 + 增益衰减 + 反馈功能,实现止痛作用。
所给化学骨架是该模板的可行示例。
1. 总体框图
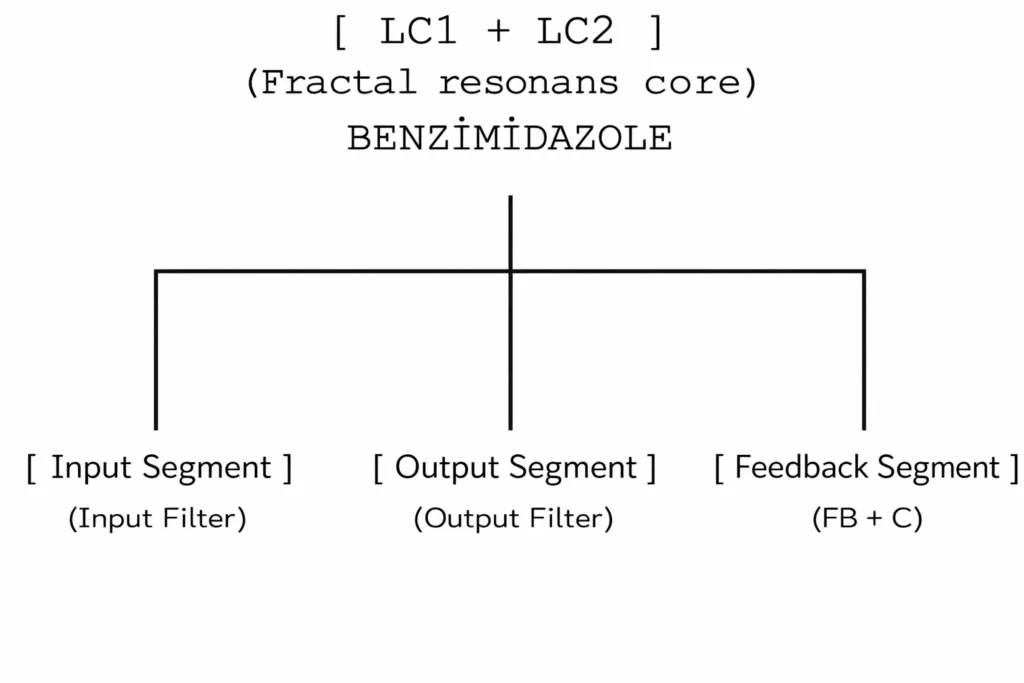
2. 入口段:磺胺+酰胺臂
化学性质:–SO2–NH–CO–CH₃
电路图:

- SO2 → 电容器 (C_in) + 二极管特性
- C=O → 二极管 (D_in)
- CH₃ → 电阻 (R_in)
3. 退出链段:酰胺+乙基支链
化学性质:–CONH–CH2CH₃
电路图:
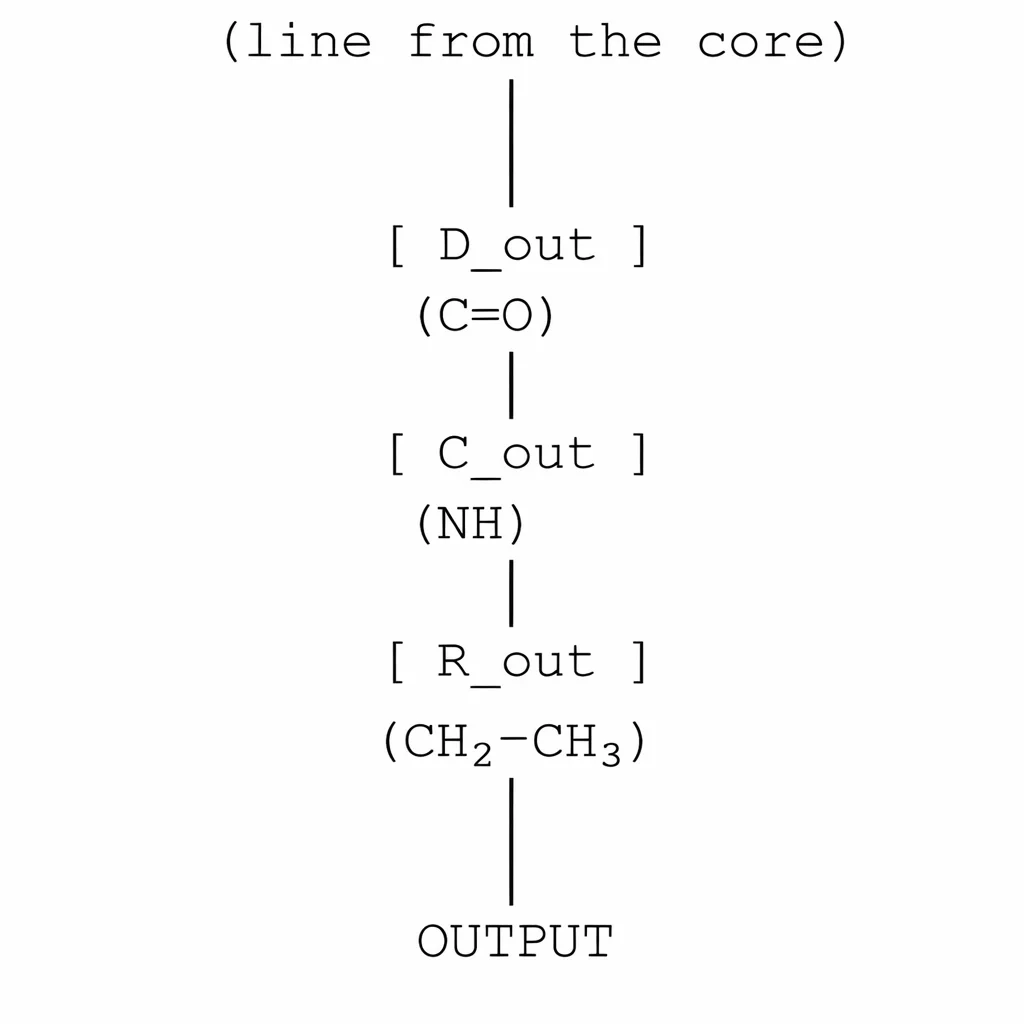
- C=O → 二极管 (D_out)
- NH→电容(C_out)+平行线电位
- 乙基 → 电阻 (R_out)
4. 反馈段:-OH分支
化学性质:-OH
电路图:

- OH → 电容器 (C_FB)
- 它还通过从核到其他片段的分子内氢键/偶极排列产生反馈效应。
5. 整个分子的电路图(整体图)
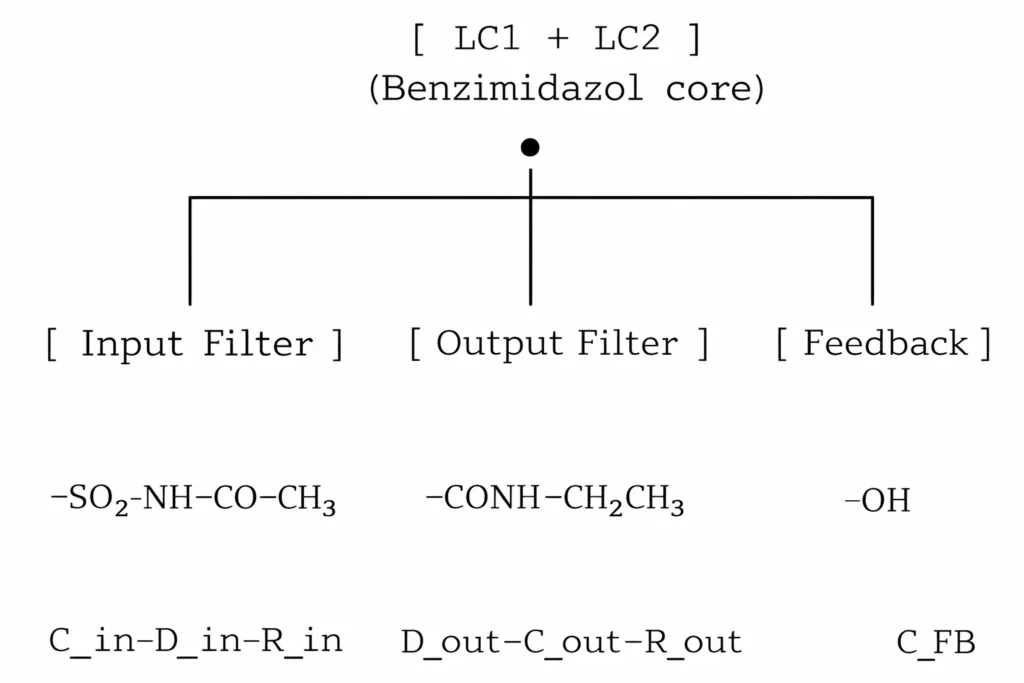
功能性阅读:
- LC1 + LC2:分形共振稳定疼痛信号。
- 输入滤波器(C_in–D_in–R_in):它平滑疼痛信号的输入峰值并限制定向流。
- 输出滤波器(D_out–C_out–R_out):重新过滤处理后的信号,降低幅度。
- 反馈(C_FB):根据其核心潜力微调整个模块的有效性。
该图是我的 FAM 模板的完整电路拓扑等效图。
比较:
| 项目 | 对乙酰氨基酚 | 阿司匹林 | 布洛芬 | 分形模块示例(苯并咪唑衍生物) |
|---|---|---|---|---|
| 中心核心 (LC) | 单苯环 → 单LC共振 | 苯 + 乙酰/羧基效应 → 单LC | 苯 + 大烷基 → 单LC,强疏水场 | 双环苯并咪唑 → LC₁ + LC₂ 分形共振 |
| 电容结构 (C) | 酚 –OH,酰胺 NH → 中/强 C | 酚 –OH + 羧基 → 强 C | 羧基 –COOH → 单一但强 C | SO₂, NH, C=O, –OH → 多个分布式电容网络 |
| 二极管结构 (D) | 酰胺 C=O → 软 D | 酯/羧基 C=O → 更尖锐 D | 羧基 C=O → 明显 D | SO₂, 两个 C=O(输入/输出),核心相互作用 → 多D网络 |
| 电阻结构 (R) | 短 CH₃ → 轻 R | 乙酰基 → 中 R | 长分支烷基链 → 强 R,疏水屏障 | CH₃, CH₂CH₃ → 可调,中等级 R(输入/输出分开) |
| 平行通路 | –NH– 桥 → 有限 | 无 N,弱,主要表面作用 | 无 N,疏水表面占主导 | 核心中 2 个 N + NH 组 → 多个受控平行通路 |
| 反馈 (FB) | 间接:共振 + 氢键 | 间接:羧基–酯平衡 | 间接:疏水分布,羧基 | 显式 FB:–OH + 分子内氢键 + 多极中心 |
| 滤波类型 | 柔和低通,中心加权 | 更尖锐低通 + 抗炎 | 强衰减器,外围加权 | 分形低通 + 双向滤波 + 反馈增益控制 |
| 分形深度 | 存在图案,但单层 | 存在图案,LC单层,C/D强 | 存在图案,R主导,LC/C/D更简单 | 在微–中–宏尺度重复相同图案 (LC+C+D+R+FB) |
| 副作用概况(电路语言) | 对肝脏回路的额外负荷(代谢电流) | 胃回路侧通道电流高 | 胃肠 + 心血管侧通道电流增加 | 理论上:目标回路高效,侧回路干扰最小化(分形选择性) |
FAM(新型分形模块)– 优势 / 劣势分析
优势
1. 分形共振深度(LC₁ + LC₂)
- 对比:对乙酰氨基酚、阿司匹林和布洛芬只使用单 LC 环。
- FAM 使用双环杂芳香核心,产生多频带共振。
- 作用:疼痛信号得到更精细、更稳定的滤波。
- 优势:→ 信号处理更稳定、更具选择性。
2. 双向滤波(输入 + 输出 电容/二极管)
- 已知止痛药的滤波是单向的。
- FAM 在输入和输出都有 C + D + R 模块。
- 优势:→ 控制疼痛信号的起点和传输 → 峰值在两阶段被平滑。
3. 反馈回路(FB)
- 对乙酰氨基酚 / 阿司匹林 / 布洛芬是被动电路。
- FAM 有主动反馈(–OH + 分子内相互作用)。
- 优势:→ 在信号过强时自动降低增益 → 减少旁路过度抑制风险。
4. 多条并联线路(||)
- 对乙酰氨基酚:1 条
- 阿司匹林:无
- 布洛芬:无
- FAM:核心 2 个 N,段内 NH,总共 3–4 条并联线路
- 优势:→ 多向连接 → 更高选择性 → 降低非靶向结合
5. 模板密度与分形同构性
- 已知止痛药含模板,但非分形。
- FAM 在微–中–宏尺度重复相同模板。
- 优势:→ 电路行为更可预测 → 分子的生物作用更一致
6. 副作用优化(电路语言)
- 阿司匹林 → 胃电路旁路电流
- 布洛芬 → 消化道 + 心血管旁路
- 对乙酰氨基酚 → 肝脏电路负载
- FAM 中:
- 电阻短且可调
- 电容分布式
- 二极管选择性
- 反馈主动
- 优势:→ 理论上最小化旁路干扰 → 最大化靶向作用
劣势
1. 化学复杂性
- FAM 含有比已知止痛药更多官能团。
- 合成与代谢路径更复杂。
- 劣势:→ 实际化学制备和代谢更困难。
2. 过敏潜力(磺酰胺段)
- 磺酰胺可能在部分人群引起过敏反应。
- 劣势:→ 小部分人群存在风险。
3. 高极性段 → 通透性可能下降
- 多个电容/二极管(SO₂, C=O, NH, OH)
- 可能影响膜穿透性
- 劣势:→ 中枢神经系统渗透减少
4. 反馈回路在生化上可能不可预测
- 电路逻辑完美
- 但生化中反馈可能高度可变
- 劣势:→ 效果因人而异
5. 疏水–亲水平衡敏感
- FAM 包含极性与非极性段
- 若平衡失调:
- 劣势:→ 可能代谢过快 → 或排泄过慢
总体结论
FAM 优势领域
- 分形共振
- 双向滤波
- 反馈
- 多条并联线路
- 高选择性
- 低旁路干扰
- 电路–分子同构
FAM 劣势领域
- 化学复杂性
- 磺酰胺过敏风险
- 通透性问题
- 代谢可预测性差
- 疏水/亲水平衡敏感

